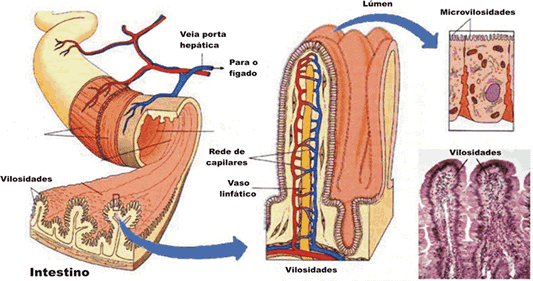
Epitelio de revestimento intestinal-ilustração
Células epiteliais intestinais: na interface da microbiota e imunidade da mucosa
Resumo
O epitélio intestinal forma uma barreira entre a microbiota e o resto do corpo. Além disso, além de atuar como uma barreira física, a função das células epiteliais intestinais (IECs) em detectar e responder aos sinais microbianos é cada vez mais apreciada e provavelmente tem inúmeras implicações para a vasta rede de células imunes dentro e abaixo do epitélio intestinal. As IECs também respondem a fatores produzidos pelas células do sistema imunológico, e estes podem regular a função de barreira, proliferação e diferenciação das IEC, além de influenciar a composição da microbiota. Os mecanismos envolvidos nas interações IEC-micróbio-imune, no entanto, não estão totalmente caracterizados. Nesta revisão, exploramos a capacidade dos IECs de direcionar a homeostase intestinal orquestrando a comunicação entre os micróbios intestinais e as células imunes adaptativas e inatas da mucosa durante condições fisiológicas e inflamatórias. Nós nos concentramos principalmente nas descobertas mais recentes e chamamos a atenção para as inúmeras incógnitas restantes sobre a complexa interferência entre IECs, a microbiota e as células imunes intestinais.
Introdução
A superfície da mucosa do trato gastrointestinal consiste em uma única camada de células epiteliais intestinais (IECs) que fornecem uma interface para que as células imunes detectem e respondam às substâncias ambientais. Estes incluem componentes alimentares e espécies microbianas patogênicas ou comensais de Archaea, bactérias, fungos, vírus e parasitas, com cerca de 10 11 bactérias colonizando o trato gastrointestinal humano. 1Isso cria uma fonte enorme de estímulos imunológicos potenciais; entretanto, sob condições homeostáticas, as células imunes na mucosa e subjacentes se desenvolvem e funcionam de maneira controlada, equilibrando as respostas inflamatórias e regulatórias para evitar a reação exagerada a antígenos luminais inócuos. Durante a infecção patogênica, as células imunes são mobilizadas para lutar e eliminar os micróbios invasores. Embora os mecanismos que regulam as respostas imunes intestinais durante a saúde e a doença ainda estejam sendo elucidados, o diálogo entre micróbios intestinais, IECs e células imunes inatas e adaptativas é cada vez mais apreciado por desempenhar um papel importante.
A monocamada IEC é composta por vários tipos de células que se diferenciam das células-tronco epiteliais que residem nas criptas. Os tipos de IEC incluem células caliciformes que produzem glicoproteínas mucinas e formam muco, enterócitos absortivos, células enteroendócrinas, células Paneth na parte inferior das criptas intestinais que secretam peptídeos antimicrobianos (AMPs), células em micro dobras (M) envolvidas na captura de antígenos e apresentação às células do sistema imunológico, e células em tufo que promovem imunidade tipo 2 aos parasitas intestinais. 2 , 3 O sequenciamento de RNA de célula única definiu ainda mais o comportamento e as características de cada tipo de célula IEC, 4 e um estudo recente identificou dois subtipos de células em tufo que mudam de frequência durante a infecção por helmintos. 5Juntos, os IECs formam a fronteira entre o corpo interno e o ambiente externo, e estudos em camundongos livres de germes demonstraram que a colonização microbiana do lúmen intestinal influencia o metabolismo, proliferação, sobrevivência, função de barreira e comunicação com células imunes de IEC. 6 IECs são o principal tipo de célula em contato direto com estímulos da microbiota luminal e são atores essenciais nas interações micróbio-hospedeiro. Como tal, além dos mecanismos de defesa mediados por células epiteliais, os IECs também coordenam o desenvolvimento e a maturação de respostas imunes a jusante de células imunes que residem na lâmina própria e nos tecidos linfoides subjacentes. Essas células imunológicas ajudam a conter os micróbios na mucosa e a manter a homeostase intestinal.
Embora muito se saiba sobre as populações de células imunes no intestino, menos se sabe sobre os mecanismos pelos quais as IECs regulam o desenvolvimento e a maturação das células imunes durante a homeostase e como isso é interrompido durante os diferentes estados de doença. Além disso, os estímulos de espécies bacterianas comensais reconhecidas por IECs e os receptores e vias de sinalização envolvidas não são totalmente compreendidos. Nesta revisão, descrevemos o papel dos IECs como importantes centros de comunicação e moduladores que moldam e coordenam a atividade de micróbios e células imunológicas. Colocamos ênfase especial nas descobertas mais recentes e destacamos as muitas questões em aberto relacionadas à complexa rede de interações entre os IECs, a microbiota e as células imunes intestinais.
Microbiota-IEC crosstalk
O epitélio intestinal é um tecido altamente dinâmico que fornece barreiras físicas e químicas para proteger a mucosa intestinal e os órgãos periféricos de micróbios comensais ou microrganismos patogênicos invasores. Além de formar uma barreira, os IECs também detectam uma miríade de sinais de micróbios intestinais, permitindo o ajuste fino da proliferação de IEC e das funções homeostáticas (Fig. 1 ). Da mesma forma, os programas de IEC podem influenciar a composição da microbiota intestinal de várias maneiras.

Regulação microbiana do crescimento e função de IEC
As células epiteliais intestinais possuem vários mecanismos para sentir e responder à presença e atividade dos micróbios intestinais. IECs expressam receptores de reconhecimento de padrões (PRRs) para detectar especificamente padrões moleculares de micróbios intestinais comensais e patogênicos, e estes foram amplamente descritos em revisões anteriores. 7 - 9 Após a detecção de micróbios intestinais, os IECs aumentam vários componentes da barreira intestinal para proteger os tecidos subjacentes do hospedeiro da infiltração bacteriana. Isso inclui a produção de AMP, secreção de muco, integridade de junção firme e crescimento e diferenciação de IEC. IECs secretam uma variedade de AMPs, muitos através de mecanismos dependentes de PRR / MyD88, que se acumulam na camada de muco e possuem ampla atividade antimicrobiana. 10, 11 De fato, durante a infecção por Citrobacter rodentium , a sinalização de MyD88 apenas em IECs foi recentemente demonstrada ser suficiente para aumentar a integridade da barreira IEC e aumentar a produção de RegIII γ e proteína sérica imunomoduladora de fase aguda amilóide A1 (SAA1). 12 As células caliciformes secretam glicoproteínas de mucina para criar a camada de muco viscosa, e a importância do muco na proteção contra micróbios invasores foi recentemente destacada em um estudo que mostra que a camada de muco descontínua no ceco do camundongo e as áreas descobertas correspondentes do epitélio formam pontos quentes para Salmonella infecção. 13Foi demonstrado que várias espécies de bactérias modulam a secreção de mucina pelas células caliciformes. Por exemplo, Ruminococcus gnavus 14 comensal e Lactobacillus rhamnosus 15 estimulam a produção de mucinas, enquanto micróbios patogênicos, incluindo Escherichia coli aderente e invasiva, promovem uma barreira de muco menos eficaz. 16 Em um estudo recente, Amuc_1100, uma proteína de membrana de Akkermansia muciniphila comensal , demonstrou interagir com o receptor PRR Toll-like 2 (TLR2) para aumentar a função de barreira intestinal, ou seja, a espessura do muco e a expressão da proteína de junção apertada (TJP). 17
Embora os mecanismos de detecção de produtos microbianos mediados por PRR sejam os mais extensivamente estudados, os IECs também usam uma série de outras vias. Por exemplo, foi demonstrado que os inflamassomas desempenham um papel importante na detecção IEC de estímulos microbianos e padrões moleculares associados a danos e no desencadeamento de respostas de barreira protetora. 18 - 21 O inflamassoma NAIP-NLRC4 foi recentemente implicado na resposta de IEC à infecção por Salmonella in vivo , permitindo programas pró-inflamatórios que resultam na produção de citocinas e da prostaglandina E 2 eicosanóide semelhante a hormônio , bem como morte de células líticas e a expulsão de IECs infectados. 22A via da autofagia também mostrou ser crítica para manter a integridade epitelial intestinal em resposta a micróbios, e um estudo recente demonstrou que a liberação de lisozima pelas células de Paneth durante a infecção bacteriana é mediada por uma via de secreção alternativa baseada na autofagia. 23 Embora os mecanismos de modulação microbiana e detecção por IECs continuem a ser descobertos, muitas vias permanecem caracterizadas de forma incompleta.
Os metabólitos microbianos produzidos pela fermentação bacteriana de componentes da dieta também são sinais importantes detectados por IECs. Por exemplo, catabólitos de triptofano, detectados pelo receptor pregnano X (PXR) 24 e o receptor de hidrocarboneto aril (AhR), 25 , 26 conduzem uma infinidade de funções de barreira antiinflamatória e protetora. A detecção IEC AhR de componentes dietéticos e catabólitos de triptofano contribui para a manutenção da integridade da barreira intestinal induzindo a diferenciação IEC de células-tronco de cripta 26 e mitigando as respostas inflamatórias. 27 PXR foi recentemente mostrado para responder ao ácido indol 3-propiônico, um metabólito de triptofano produzido por esporogenes de Clostridium comensal, e os camundongos deficientes para PXR exibiram aumento da lesão inflamatória epitelial e diminuição da expressão da proteína de junção apertada. Em contraste, camundongos livres de germes colonizados com C. sporogenes e doseados com 1- triptofano exibiram diminuição da permeabilidade intestinal e aumento da expressão de desintoxicação de genes alvo de PXR. 24 Além de servir como uma importante fonte de energia para enterócitos, os ácidos graxos de cadeia curta derivados da microbiota (SCFAs) também foram implicados na regulação da maioria das funções de IEC, incluindo renovação celular, 28 expressão de proteína de junção apertada, 29 e inflamassoma- ou integridade epitelial mediada pelo fator indutível por hipóxia (HIF). 30 , 31Os SCFAs podem influenciar diretamente a transcrição do gene ligando-se e inibindo as histonas desacetilases (HDAC) ou ligando-se aos receptores sensíveis ao metabólito GPR41, GPR43 e GPR109A. 32 De fato, um estudo recente mostrou que a expressão ideal de AMPs requer a detecção de IEC de SCFAs via GPR43. Usando Gpr43 - / - camundongos e enteróides, os pesquisadores observaram que os AMPs RegIII γ e β- defensinas 1, 3 e 4 foram reduzidos na ausência de GPR43 ou alvo mamífero a jusante de rapamicina (mTOR) e transdutor de sinal e ativador de transcrição 3 ( STAT3) ativação. 33
Os micróbios também induzem uma série de funções não-barreira em IECs, incluindo mudanças no metabolismo e na biossíntese de moléculas de sinalização. Por exemplo, no início da infecção por Citrobacter rodentium , os IECs mostraram exibir mudanças nas vias metabólicas do colesterol e do carbono, sugerindo que o metabolismo do IEC é reprogramado para atender ao aumento da demanda energética celular durante o reparo do tecido. 34 Foi demonstrado que algumas células enterocromafins, um subtipo de célula enteroendócrina, secretam serotonina (5-hidroxitriptamina, 5-HT) em resposta ao mecanossensibilização através do mecanotransdutor Piezo2, 35 e 5-HT é um importante regulador do desenvolvimento do sistema nervoso entérico, e motilidade e inflamação do trato gastrointestinal. 36Além do mecanosenseamento, um estudo recente demonstrou que vários metabólitos de um consórcio de bactérias formadoras de esporos comensais (predominantemente espécies de Clostridium) promovem a biossíntese de 5-HT por células enterocromafins colônicas em camundongos colonizados. 37 Em resposta aos micróbios, os IECs também secretam várias citocinas e moléculas efetoras, incluindo interleucina-25 (IL-25) e SAA. 38 , 39 Esses efetores regulam o desenvolvimento e a função das células imunes intestinais, conforme descrito na próxima seção desta revisão. Coletivamente, essas descobertas recentes indicam que uma ampla gama de funções IEC são afetadas pela detecção de micróbios intestinais (Tabela 1); no entanto, é importante notar que muitos desses estudos foram realizados no contexto de infecção microbiana patogênica. Mais estudos são necessários para identificar estímulos adicionais de micróbios comensais e caracterizar respostas de IEC comensuráveis no estado estacionário.
| Sensor IEC / via de sinalização | Estímulos microbianos | Espécies microbianas usadas | In vivo / in vitro e detalhes do estudo | Resposta IEC | Referências |
|---|---|---|---|---|---|
| Receptor 9 semelhante a Toll, fator nuclear κB | DNA bacteriano CpG não metilado 1 | Citrobacter rodentium (DBS100), Salmonella typhimurium (ATCC 14028), Helicobacter pylori (PMSS1) | In vivo, a TLR9 - / - murganhos | Diminui a inflamação intestinal e os danos após o desafio bacteriano | 140 - 143 1 |
| Apoptose mediada por caspase-3/7 | Enterotoxinas (TcdA e TcdB) | Clostridium difficile (VPI10463) | Organóides intestinais in vivo e in vitro ; CASP3 / 7 IEC-KO murganhos | Restringe o crescimento de C. difficile in vivo | 144 |
| NAIP / NLRC4 inflamassoma | Flagelina 1 Desconhecido 2 | Salmonella Typhimurium, Citrobacter rodentium 2 | In vivo, Casp1 - / - , Casp8 - / - , Nlrc4 - / - | Protege contra a invasão de patógenos entéricos; expulsão de IECs piroptóticos e liberação de eicosanóide e interleucina-18 (IL-18) | 21 , 22 , 145 1 |
| Receptor tipo Toll 4, receptor ativado por proliferador de peroxissoma (PPAR) | Ácidos graxos livres 1 | Micróbios intestinais comensais | In vivo , Tlr4 IEC-KO | Previne o desenvolvimento da síndrome metabólica; regula a expressão de lisozima e genes controlados por PPAR | 58 , 146 , 147 1 |
| Inflamasoma P2X7R / NLRP3 | Ligantes incluem ATP extracelular e K + 1 | Toxoplasma gondii | In vitro , células FHs 74 Int | Secreção de IL-1 β e inibição da proliferação parasitária | 18, 148, 1491 |
| NLRP6 inflammasome | Unknown | Citrobacter rodentium | In vivo, Nlrp6−/−, Asc−/−, Casp1/11−/− | Orchestrates goblet cell mucin granule exocytosis | 19 |
| Nlrp9b inflammasome | dsRNA1 | Rotavirus EW | In vivo, Nlrp9b−/−, Nlrp9bIEC-KO | Restricts rotavirus infection by IL-18 production and pyroptosis | 20 |
| Aryl hydrocarbon receptor | Tryptophan indole derivatives | Lactobacilli, Clostridiales members | In vivo, Ahr−/− | IL-22 production; resistance to enteric pathogens; maintenance of intestinal homeostasis and barrier functions | 25-27 |
| Receptors GPR41, GPR43 and GPR109; HDAC inhibition; mTOR, STAT3, ERK and MAPK signalling | short-chain fatty acids | Various microbes including Bacteroides spp. | In vivo, GPR41−/−, GPR43−/−, GPR109−/−, in vitro murine intestinal organoids | Protective inflammatory responses during pathogen infection; secretion of AMPs, chemokines and cytokines; controls IEC turnover and barrier functions; RALDH1 expression and vitamin A metabolism | 28-31, 33, 150-152 |
| MyD88 signalling | Various TLR ligands | Citrobacter rodentium | In vivo, MyD88−/− | Secretion of AMPs, control of bacterial infiltration, enhanced barrier integrity | 12 |
| GPCR and ERK/MAPK signalling | Pili, novel 3000 MW molecule | Lactobacillus rhamnosus (CNCM I-3690), Ruminococcus gnavus (E1) | In vivo, in vitro HT29-MTX cells | Expression of glycoroteins and mucus production by goblet cells; cytoprotective responses | 14, 15 |
| Various cellular stresses including nutrient deprivation, infection with microbes1 | Autophagy | Helicobacter hepaticus, Salmonella Typhimurium, Pasteurellaceae family | In vivo, Atg161−/−, in vitro Atg161−/− organoids | Control inflammation-induced apoptosis, necroptosis and maintains intestinal barrier, lysozyme secretion by Paneth cells, promotes bacterial clearance | 23, 43, 45, 153-155 1 |
| Cellular forces | Mechanosensors/mechanotransducer Piezo2 | Clostridial species | In vivo, in vitro | Serotonin release by enterochromaffin cells | 35, 37 |
| Peptidoglycan components; muramyl dipeptide1 | Nod2 | Bacteroides vulgatus, Enterococcus faecium | In vivo, Nod2−/− and in vitro | Restriction of bacterial growth or dissemination, expression of inflammatory genes, goblet cell function | 56 , 156 , 157 1 , 158 |
| Receptor de pregnano X (PXR) | Ácido indol 3-propiônico | Clostridium sporogenes | In vivo , Nr1i2 - / - , Nr1i2 - / - , Tlr4 - / - , Pxr - / - | Regulação da permeabilidade intestinal e inflamação intestinal, defesa contra patógenos intracelulares | 24 , 159 |
- 1 Um achado de um estudo diferente ou adicional.
- 2 Embora se acredite que os componentes do sistema de secreção do tipo 3 expressos por C. rodentium forneçam o estímulo que desencadeia a formação do inflamassoma de NLRC4 in vivo , isso ainda não foi demonstrado.
Influência de IECs na diversidade e função da microbiota intestinal
Embora os efeitos da interferência do micróbio IEC em IECs estejam começando a ser elucidados, os efeitos dessa interação na microbiota intestinal são substancialmente menos caracterizados. Ainda assim, vários estudos recentes indicaram que os IECs também têm um impacto nas populações microbianas que residem no intestino. A autofagia é particularmente bem estudada na manutenção da função das células de Paneth e na proteção contra bactérias patogênicas. 40 - 44 Recentemente, a interrupção da autofagia IEC também mostrou alterar dramaticamente a composição da microbiota intestinal e reduzir a diversidade alfa microbiana intestinal em camundongos. 45 Outro estudo recente mostrou que a produção de serotonina por células enterocromafins modula a composição microbiana intestinal, 46e os AMPs secretados por IECs têm sido amplamente relatados como influenciando a composição dos micróbios intestinais. 47 - 49 O NLRP6-inflamassoma também é altamente expresso por IECs, e estudos anteriores mostraram que o NLRP6 ajuda a manter a eubiose da microbiota intestinal. 50 , 51 No entanto, estudos recentes de camundongos Nlrp6 - / - e Asc - / - co-alojados com companheiros de ninhada de tipo selvagem relatam que o inflamassoma de NLRP6 não afeta a diversidade microbiana do intestino, 52 , 53 destacando que fatores de confusão não genéticos podem impactar na Vivoestudos que investigam relações causais entre deficiências do gene do hospedeiro e alterações na microbiota. 54 De fato, enquanto os estudos anteriores eliminaram um papel para a proteína 1 contendo o domínio de oligomerização de ligação de nucleotídeos (NOD1) e NOD2 na formação da composição da microbiota com base na reação em cadeia da polimerase para 10 grupos bacterianos direcionados em companheiros de ninhada co-alojados de diferentes genótipos, 55 sinalização de NOD2 em IECs foi recentemente fortemente implicado no controle específico da colonização e crescimento de Bacteroides vulgatus comensais . 56 Neste estudo recente, embora os animais do tipo selvagem co-alojados com camundongos Nod2 - / - tenham adquirido a superabundância de B. vulgatuscaracterística de camundongos knockout, isso diminuiu após a nova separação. Dadas essas observações conflitantes, um caso forte foi feito para o uso de cruzamentos e controles de companheiros de ninhada como uma alternativa superior (ou adição) ao co-alojamento. 57 Ainda assim, os efeitos dos PRRs de IEC sobre a composição da microbiota intestinal permanecem controversos e, mais importante, os mecanismos por trás de muitas das alterações da microbiota observadas não foram totalmente descobertos.
A expressão de genes microbianos também é influenciada por IECs por meio de vários mecanismos. Por exemplo, um estudo recente usando camundongos nocaute de TLR4 específico para IEC (TLR4 IEC-KO ) demonstrou que TLR4 influencia a composição e função de micróbios intestinais, incluindo a expressão de genes microbianos envolvidos no metabolismo de lipídios, aminoácidos e nucleotídeos. 58 Camundongos TLR4 IEC-KO desenvolveram síndrome metabólica, e a lisozima e os genes regulados por receptores ativados por proliferadores de peroxissoma foram regulados negativamente, sugerindo um mecanismo pelo qual o TLR4 intestinal pode influenciar a microbiota. Em outro estudo, anexar e apagar E. coli enterohemorrágicademonstrou requerer mecanosenseamento de IECs para expressar o locus de apagamento de enterócitos que codifica seu sistema de secreção tipo 3, e este foi responsável pela formação de lesões no trato gastrointestinal. 59 Além disso, um estudo recente relatou que o miRNA é liberado por IECs no lúmen intestinal, onde entra em espécies bacterianas como Fusobacterium nucleatum e E. coli e regula sua expressão gênica e crescimento. 60
A principal fonte de nutrientes para os micróbios intestinais são normalmente componentes derivados da dieta, incluindo polissacarídeos ou glicanos. No entanto, alguns micróbios intestinais também podem usar glicanos hospedeiros nas proteínas mucinas e na superfície de IECs, fornecendo uma fonte de energia alternativa quando os glicanos dietéticos são reduzidos. 61 - 63 Por exemplo, vários membros comensais de Clostridiales usam os açúcares fucose e ácido siálico associados à mucina como fontes de energia, promovendo sua colonização intestinal. 27 Os glicanos também são ligantes da fixação bacteriana, e algumas espécies microbianas intestinais, como Ruminococcus gnavus, têm como alvo a mucina glicana para auxiliar sua disseminação e persistência em nichos no lúmen intestinal. 64 Juntos, esses estudos demonstram a multiplicidade de interações entre micróbios e IECs que podem desencadear vários programas de IEC e moldar o ecossistema microbiano no intestino.
IEC-crosstalk de célula imune
As células epiteliais intestinais possuem uma série de funções de barreira independentes para controlar e / ou matar micróbios intestinais, elas também medeiam a interferência entre a microbiota e as células imunes intraepiteliais e subepiteliais, respondendo a metabólitos microbianos e coordenando as respostas imunes. Isso é obtido por uma série de mecanismos conhecidos e desconhecidos, incluindo a secreção de quimiocinas, citocinas e outras moléculas imunomoduladoras (Fig. 2 ), bem como o transporte de antígenos microbianos e metabólitos para células imunes subjacentes na lâmina própria. Reciprocamente, as células imunes intestinais suportam uma série de funções IEC importantes (Fig. 3 ).


Secreção IEC de moléculas imunomoduladoras
Entre as moléculas imunomoduladoras que são produzidas por IECs, a linfopoietina estromal tímica, o fator de crescimento transformador (TGF) - β , o ácido retinóico e a IL-10 mostraram impactar uma ampla gama de células imunológicas e cada um ganhou suas próprias revisões detalhadas. 65 - 68 Além desses moduladores bem descritos da função de células imunes, a produção de IEC de IL-15 foi recentemente demonstrada ser necessária para o homing de linfócitos intraepietílicos receptor- γδ- positivo de células T protetor (TCR- γδ + ) (IELs) para o epitélio do intestino delgado. 69 O TCR- γ δ +O comportamento de vigilância IEL, respostas antimicrobianas e proteção contra patógenos como Salmonella Typhimurium e Toxoplasma gondii são dependentes da sinalização MyD88 em IECs; 70 , 71 no entanto, os mecanismos de comunicação IEC-IEL necessários para essas funções ainda são desconhecidos. Em resposta à colonização por microrganismos aderentes, IECs secretam AEA, que promove a maturação funcional do retinóico relacionadas com o ácido orphan receptor γ t-positivo (ROR γ t + células T) de IL-17, secretoras de tipo T helper 17 células (Th17) . 72 , 73Foi hipotetizado que isso ocorreria por meio de mecanossensibilização de contato microbiano, e um estudo recente mostrou que, no caso de bactérias filamentosas segmentadas (SFB), a transferência de antígenos SFB através de IECs via endocitose desencadeada por adesão microbiana (MATE) desempenha um papel fundamental . 74 Outro estudo recente mostra que a detecção epitelial da vitamina A da dieta por meio do receptor de ácido retinóico β também é necessária para a expressão de IEC de SAAs. 75
Talvez menos apreciados, os glicocorticóides (GCs) e neurotransmissores também são abundantemente produzidos por células epiteliais no intestino. Os GCs são bem conhecidos por seus efeitos antiinflamatórios gerais, mas além de sua produção nas glândulas supra-renais, as criptas IECs têm demonstrado liberar GCs em resposta à ativação de células T mediada por anti-CD3, e a síntese de GCs por IEC foi demonstrada para controlar a inflamação local e a gravidade da doença em um modelo de colite com ácido 2,4,6-trinitrobenzeno sulfônico. 76 , 77Como quase todas as células de vertebrados expressam receptores de glicocorticóides (GRs), os efeitos dos GCs são pleiotrópicos; no entanto, foi demonstrado que as respostas específicas das células T aos GCs estão envolvidas na homeostase das células T, e recentemente foi demonstrado que a deficiência regulatória de GR específica das células T (Treg) prejudica a capacidade das células Treg de prevenir a indução de doença em um camundongo modelo de doença inflamatória intestinal. 78 , 79 Além disso, um estudo recente de camundongos com respostas reduzidas de GR revelou uma assinatura de gene específico do interferon no intestino que foi anulada pelo tratamento com antibióticos, indicando um papel para a microbiota. 80 Embora as informações sobre a produção intestinal de GCs continuem a emergir, os estímulos envolvidos e os efeitos das células imunológicas ainda não foram totalmente elucidados.
Da mesma forma, embora seja um neurotransmissor monoamina, a serotonina é produzida principalmente nos intestinos pelas células enterocromafins. Conforme discutido anteriormente, um estudo recente usando camundongos livres de germes colonizados com bactérias formadoras de esporos identificou um papel para metabólitos de micróbios comensais na promoção da biossíntese de serotonina por células enterocromafins colônicas. 37 Embora os efeitos da serotonina nas células imunes intestinais não tenham sido completamente caracterizados, a maioria das células imunes expressa o transportador de serotonina (SERT), e há evidências de que funções tão diversas como ativação de células T, tráfico de eosinófilos e fator de necrose tumoral- α - a inflamação mediada é modulada pela serotonina. 81 - 83
Transporte IEC de antígenos microbianos e metabólitos
Um mecanismo importante pelo qual as células epiteliais intestinais dirigem as respostas imunes adaptativas aos micróbios intestinais é por amostragem de antígeno e apresentação às células imunes subjacentes ao epitélio. As células M especializadas estão concentradas no epitélio associado ao folículo que recobre a superfície luminal das placas de Peyer e os folículos linfoides isolados do intestino delgado. As células M captam diretamente antígenos e microrganismos intactos do lúmen intestinal e os transportam de forma unidirecional para apresentação às células imunes residentes. A amostragem de antígeno por células M é provavelmente o iniciador chave das respostas de IgA intestinal às bactérias comensais, uma vez que camundongos com diferenciação de células M prejudicada exibem IgA secretora fecal diminuída. 84
Além das células M, as células caliciformes contribuem para a amostragem de antígenos, formando passagens de antígenos associados a células caliciformes (GAPs) para fornecer antígenos do lúmen intestinal às células dendríticas CD103 + na lâmina própria. 85 A regulação dos GAPs pode constituir um meio dinâmico de modular as respostas imunes intestinais. Enquanto as células caliciformes do intestino delgado formam GAPs em resposta à acetilcolina, a detecção de células caliciformes do cólon de micróbios comensais via MyD88 diminui sua responsividade à acetilcolina e a formação de GAPs para limitar as respostas imunes inflamatórias aos comensais. 86 O controle cronometrado de GAPs durante a fase de pré-desmame foi implicado na tolerância mediada por células Treg a bactérias comensais, 87 e durante Salmonellainfecção IL-1 β inibe a formação de GAP, levando à diminuição da disseminação bacteriana. 88
Os enterócitos também participam da apresentação de antígenos por vários processos. Estes incluem a apresentação de antígenos lipídicos para células T assassinas naturais através da expressão de CD1d, e a expressão de IEC CD1d demonstrou suprimir funções de células T assassinas naturais pró-inflamatórias, reduzindo assim a inflamação intestinal. 89 Além disso, o MHC de classe II demonstrou ser expresso constitutivamente por IECs nas vilosidades superiores do intestino delgado, e a expressão de superfície parece estar aumentada em pacientes com doença inflamatória intestinal e em resposta ao interferon- γ . 90 - 92 Reciprocamente, a apresentação do antígeno IEC mostrou promover a secreção de interferon- γ por CD4 +Células T em co-culturas de células T normais com IECs de pacientes com doença inflamatória intestinal; 93 no entanto, estudos mais recentes sugerem que a expressão de MHC de classe II induzida por interferon-γ em IECs desempenha um papel mais antiinflamatório, promovendo uma proporção tolerogênica de células Treg para células T CD4 + efetoras . 94 , 95 Ainda assim, o papel da apresentação do antígeno IEC na formação da imunidade intestinal não foi completamente explorado, e o contato íntimo entre o epitélio e os micróbios comensais fornece ampla oportunidade para os IECs curarem as respostas das células T intestinais.
Contribuições de células imunológicas para a diferenciação e função de IEC
Além das IECs que regulam as funções das células imunes, vários tipos de células imunes intestinais influenciam a homeostase das IEC e as respostas inflamatórias (Fig. 3 ). Por exemplo, em resposta a metabólitos microbianos, como catabólitos de triptofano, as células linfoides inatas tipo 3 (ILC3s) produzem citocinas que regulam as funções de barreira das IECs. 25 ILC3s secretam IL-22, que promove a homeostase e reparo de IEC, e pode induzir AMPs a controlar o crescimento de micróbios patogênicos e comensais. 96 - 98 de IL-22 afecta também a glicosilação de proteínas de superfície IEC através da indução de expressão fucosiltransferase 2 (FUT2), aumentando assim a protecção do hospedeiro contra a Salmonella Typhimurium. 99A produção de mucina por IECs também é aumentada por IL-22 através da ativação do transdutor de sinal e ativador da transcrição STAT3, 100 e proteínas de junção apertada, como claudina-2, recentemente mostraram ser reguladas positivamente por IL-22, induzindo diarreia e facilitando a depuração de Citrobacter rodentium em um modelo de camundongo com infecção entérica. 101
Além de ILC3s e IL-22, algumas outras células linfóides também contribuem para as respostas de IEC. Durante a infecção parasitária, IECs secretam uma série de citocinas que promovem a expansão e ativação de células linfoides inatas do grupo 2 (ILC2s) e basófilos, incluindo IL-33 e linfopoietina estromal tímica (TSLP) e IL-25 produzida por células em tufo. 2 , 5 , 102 , 103 Reciprocamente, ILC2s ativados secretam IL-13, que promove a diferenciação de células em tufos e caliciformes e eliminação do parasita. 3 , 104 As citocinas de assinatura secretadas pelas células Th17 (IL-17A, IL-17F e IL-22) também podem induzir a secreção de AMP mediada por IEC e reforçar as junções estreitas de IEC. 105 - 108Além disso, a produção de fator de crescimento de fibroblastos 2 (FGF2) por células Treg demonstrou recentemente sinergia com IL-17 para aumentar os mecanismos de reparo epitelial intestinal. 109 A responsividade do IEC ao fator de necrose tumoral também promove o reparo da mucosa e a cura em indivíduos com doença de Crohn, células humanas e modelos de camundongos. 110
As células mieloides também desempenham papéis importantes na diferenciação e função de IEC. Por exemplo, perturbações nas interações macrófago-IEC levam à diferenciação aberrante de subtipos IEC. Usando o bloqueio de CSF1R para depletar macrófagos que se localizam no epitélio da cripta intestinal, um estudo recente descobriu que a ausência de macrófagos resulta em células-tronco intestinais Lgr5 + reduzidas , células de Paneth que expressam lisozima e células M do patch de Peyer e aumento da densidade de células caliciformes. 111 Os macrófagos também mostraram ser a fonte provável de IL-10 em um modelo de lesão induzida por biópsia do cólon e, neste modelo, a síntese epitelial induzida por macrófago IL-10 da proteína de sinalização induzível por WNT1 pró-reparo 1 para mediar IEC proliferação e cicatrização de feridas na mucosa. 112Em DCs, a sinalização do fator de crescimento transformador- β foi sugerida para controlar o número de células caliciformes, a produção de muco e a gravidade da doença na colite de sulfato de sódio dextrana via sinalização Notch, embora os efeitos da disfunção das DC e envolvimento de outros tipos de células imunes não tenham sido totalmente investigados em este estudo. 113 Mais recentemente, a responsividade da IL-12 via IL-12R β 2 em IECs demonstrou desempenhar um papel protetor na alergia alimentar; no entanto, o mecanismo preciso de proteção é mais uma vez desconhecido. 114
Célula imune-crosstalk microbiota
Devido ao contato direto limitado, a maior parte da comunicação célula-microbiota do sistema imunológico é provavelmente mediada, pelo menos até certo ponto, por IECs; no entanto, as contribuições das IECs para muitas interações microbiota-células imunes ainda precisam ser totalmente realizadas. No entanto, um crescente corpo de trabalho revelou a importância dos micróbios comensais para o desenvolvimento e função adequados das células imunes (Fig. 4 ), e as células imunes reciprocamente moldam o habitat microbiano e a diversidade da microbiota.

Modulação da microbiota de linfócitos intestinais
Como mencionado anteriormente, o desenvolvimento adequado de células Th17 secretoras de IL-17 requer a produção de SAA por IECs em resposta à adesão microbiana e especificamente MATE em resposta à adesão de SFB. O simbionte humano Bifidobacterium adolescentis , que se associa intimamente com o epitélio intestinal, também induz células Th17 no intestino murino com um programa de transcrição distinto de SFB, sugerindo que o acúmulo de Th17 também pode ser promovido por outro mecanismo. 115Embora papéis precisos para IECs não tenham sido completamente definidos, papéis para metabólitos microbianos comensais e antígenos também continuam a emergir para a geração e função de células Treg. Em três estudos seminais, o butirato derivado do comensal demonstrou conduzir a indução de células Treg periféricas no cólon. 116 - 118 Um estudo posterior também mostrou um papel para o reconhecimento de antígenos de micróbios comensais na diferenciação de células Treg intestinais. A transferência de células T transgênicas ingênuas específicas para antígenos comensais em camundongos com uma microbiota normal resultou na indução de Foxp3 robusta nessas células. 119 No desmame, a microbiota intestinal induz uma resposta imune vigorosa associada à geração de ROR γ t +Células Treg de uma maneira dependente de SCFA e ácido retinóico, e a inibição dessa resposta leva a imunopatologias posteriores, incluindo colite. 120
ROR γ t + Treg células específico para Helicobacter hepaticus também demonstraram tolerância mediata para este pathobiont comensais, 121 e um polissacárido da mesma espécie induz anti-inflamatório de IL-10 em macrófagos secreção intestinal. 122 No entanto, a especificidade do Helicobacter em si não dita um programa antiinflamatório. Um estudo recente demonstrou que as mesmas células T específicas do Helicobacter se diferenciam em células Treg durante a homeostase e células T efetoras durante a colite. 123 Helicobacter bilisa colonização, por outro lado, mostrou previamente induzir reatividade imunológica persistente a outras bactérias comensais. 124 Coletivamente, esses estudos sugerem a importância de pistas contextuais independentes do antígeno durante a ativação das células T no intestino para determinar o destino das células T. De fato, dois ácidos biliares secundários, gerados pela transformação de ácidos biliares primários por bactérias comensais, mostraram recentemente inibir a diferenciação Th17 e promover a indução de células Treg. 125 A identificação de todo o espectro de pistas contextuais será fundamental para a compreensão de como as células T intestinais são programadas.
Além das células T convencionais, os IELs provaram ser marcadamente influenciados pela microbiota comensal. Por exemplo, TCR- αβ + IELs estão quase ausentes em camundongos livres de germes, 126 , 127 e TCR- γδ + IELs têm atividade citolítica prejudicada. 128 Os mecanismos desse controle ainda estão sob investigação, mas provavelmente envolvem a transmissão de sinais por meio dos IECs. A microbiota intestinal também é um fator importante na geração de TCR- αβ + CD4 + CD8 αα + IELs. Em um estudo recente, a introdução de Lactobacillus reuteri, que metaboliza o triptofanoem camundongos que receberam uma dieta rica em triptofano foi suficiente para induzir a diferenciação de TCR αβ + CD4 + CD8 αα + IEL. 129 Outro estudo demonstrou a conversão dependente da microbiota de células da lâmina própria Foxp3 + Treg em TCR αβ + CD4 + CD8 αα + IELs após o direcionamento para o epitélio intestinal. 130 A capacidade das células epiteliais e metabólitos microbianos de contribuir para a indução desse subconjunto IEL também está sendo elucidada.
Efeitos das células imunológicas na microbiota intestinal
Embora historicamente enfrentado com ceticismo e comparativamente pouco estudado, as influências das células do sistema imunológico intestinal sobre a microbiota também estão ganhando destaque. A evidência de que o sistema imune adaptativo modela a composição e diversidade microbiana no intestino foi fornecida usando o sequenciamento de bactérias em múltiplos loci intestinais em camundongos com deficiência de Rag que carecem de células B e T. 131 No entanto, enquanto ILCs estão presentes em camundongos com deficiência de Rag, há evidências de que seu número e função estão alterados, 132complicando as conclusões que podem ser tiradas desses animais sobre o papel das células B e T. Outros estudos identificaram um papel importante para a IgA polirreativa em facilitar a indução de IgA específica para bactérias, e as diferenças entre elas influenciam significativamente a colonização por micróbios comensais. 133 Na verdade, Bacteroides fragilis agora demonstrou permitir a ligação de IgA para facilitar sua capacidade de ocupar um nicho intestinal privilegiado nas proximidades de IECs. 134 Muito recentemente, um papel importante foi identificado para IgG específico comensal que resulta de ruptura epitelial no intestino. A capacidade de resposta a esses IgGs em macrófagos intestinais por meio da ativação de Fc γ Rs conduz a inflamação intestinal e a colite.135 Embora os efeitos dessas IgGs na composição da microbiota ainda não tenham sido caracterizados, estudos futuros podem definir funções para IgA e IgG intestinal na modulação de comunidades microbianas comensais.
As células imunológicas no intestino têm a tarefa de manter um equilíbrio entre a inflamação fisiológica e a tolerância. Os programas de células imunes intestinais resultantes regulam o ecossistema microbiano no intestino de uma maneira que permite a colonização benéfica e impede a infecção patogênica invasiva. Por exemplo, foi demonstrado que as células Foxp3 + Treg suportam a diversidade da microbiota suprimindo a inflamação e facilitando a seleção de IgA nas placas de Peyer. 136 Por outro lado, a falta de células Treg periféricas leva ao aumento das respostas imunes tipo 2 e à interrupção de nichos microbianos para bactérias que vivem na fronteira de IEC, 137destacando a importância dessas células T na formação do ambiente microbiano intestinal. Além da composição e diversidade, a evolução das espécies bacterianas comensais também mostrou ser influenciada pela imunidade adaptativa do hospedeiro. Nos intestinos de camundongos com deficiência de Rag, a taxa e a previsibilidade da adaptação de E. coli são alteradas em comparação com os hospedeiros do tipo selvagem. 138 Tomados em conjunto, esses estudos trazem novos insights sobre a interdependência íntima da microbiota intestinal e do sistema imunológico e abrem questões adicionais sobre os mecanismos envolvidos e a contribuição dos IECs.
Conclusão
Devido à localização anatômica das IECs entre a microbiota intestinal e os tecidos intestinais do hospedeiro, é razoável prever que as IECs desempenham um papel importante no controle da interação entre a microbiota luminal e as células imunes subjacentes. De fato, a literatura recente destacou a capacidade dos IECs de contribuir para moldar a imunidade intestinal do hospedeiro e a composição microbiana intestinal. No entanto, apesar dos avanços recentes na área, vários desafios ainda precisam ser enfrentados e superados.
Demonstrou-se que é difícil demonstrar que os fatores secretados por IEC são induzidos em resposta a sinais derivados de micróbios e os efeitos desses fatores nas células do sistema imunológico. A maioria das citocinas derivadas de IEC também são produzidas por outros tipos de células, portanto, o envolvimento de IEC in vivo é geralmente inferido, mas não definitivamente demonstrado. Camundongos knockout para certos receptores ou moléculas efetoras expressas por IECs produziram uma visão mais aprofundada dos papéis dos IECs como sensores diretos de sinais microbianos; no entanto, poucos estudos empregaram a ablação genética específica de IEC in vivo. O estudo do impacto da sinalização de micróbio-IEC na função de subconjuntos de células imunes também é limitado devido à dificuldade em isolar e manipular esses tipos de células; a vida útil dos IECs é extremamente curta, pois eles são renovados a cada 2–6 dias. 139 Embora os modelos in vitro tenham fornecido informações valiosas sobre as vias de sinalização IEC e a produção de efetores, eles permanecem incapazes de recapitular a complexidade do ambiente intestinal, e a interpretação desses estudos é consequentemente limitada. Ao elucidar ainda mais os mecanismos envolvidos no crosstalk micróbio-imune no epitélio intestinal, podemos entender melhor o papel dos IECs na regulação da imunidade do hospedeiro durante a homeostase, bem como durante os estados de disbiose e doença.
Divulgações
A VAP é apoiada pela Royal Society and Wellcome Trust, Sir Henry Dale Fellowship. Os autores declaram não haver conflito de interesses.
Referências
- Um , , . Estimativas revisadas para o número de células humanas e de bactérias no corpo . PLoS Biol 2016 ; 14 : e1002533.
- 2 , , , . A IL-25 derivada de células de tufo regula um circuito de resposta epitelial intestinal ILC2 . Nature 2016 ; 529 : 221 - 5 .
- 3 , , , , , et al . Células de tufo, células quimiossensoriais gustativas, orquestram a imunidade do parasita tipo 2 no intestino . Science 2016 ; 351 : 1329 - 33 .
- 4 , , , , , et al . Diversidade de células epiteliais do cólon na saúde e doença inflamatória intestinal . Nature 2019 ; 567 : 49 - 55 .
- 5 , , , , , et al . Um levantamento unicelular do epitélio do intestino delgado . Nature 2017 ; 551 : 333 - 9 .
- 6 , , . Uso de animais axênicos no estudo da adaptação de mamíferos à sua microbiota intestinal comensal . Semin Immunol 2007 ; 19 : 59 - 69 .
- 7 , , , . O microbioma e a imunidade inata . Nature 2016 ; 535 : 65 - 74 .
- 8 , . O reconhecimento imunológico inato da microbiota promove a simbiose hospedeiro-microbiana . Nat Immunol 2013 ; 14 : 668 - 75 .
- 9 . Reconhecimento de células epiteliais de bactérias comensais e manutenção da homeostase imunológica no intestino . Nat Rev Immunol 2008 ; 8 : 411 - 20 .
- 10 , , , , . As células Paneth detectam diretamente os comensais intestinais e mantêm a homeostase na interface intestinal hospedeiro-microbiana . Proc Natl Acad Sci USA 2008 ; 105 : 20858 - 63 .
- 11 , , , . Aumento da expressão de peptídeos antimicrobianos e lisozima em células epiteliais do cólon de pacientes com colite ulcerativa . Clin Exp Immunol 2003 ; 131 : 90 - 101 .
- 12 , , , , , et al . A sinalização MyD88 nas células dendríticas e no epitélio intestinal controla a imunidade contra a infecção intestinal por C. rodentium . PLoS Pathog 2017 ; 13 : e1006357.
- 13 , , , . A arquitetura do muco e a natação próxima à superfície afetam os padrões distintos de infecção por Salmonella typhimurium ao longo do trato intestinal murino . Cell Rep 2019 ; 27 : 2665 - 78 e3.
- 14 , , , , , et al . Ruminococcus gnavus E1 modula a expressão da mucina e a glicosilação intestinal . J Appl Microbiol 2016 ; 120 : 1403 - 17 .
- 15 , , , , , et al . O potencial probiótico Lactobacillus rhamnosus CNCM I-3690 cepa protege a barreira intestinal, estimulando a produção de muco e a resposta citoprotetora . Sci Rep 2019 ; 9 : 5398 .
- 16 , , , , , et al . A protease Vat-AIEC promove o cruzamento da camada de muco intestinal por Escherichia coli associada à doença de Crohn . Cell Microbiol 2016 ; 18 : 617 - 31 .
- 17 , , , , , et al . Uma proteína de membrana purificada de Akkermansia muciniphila ou a bactéria pasteurizada melhora o metabolismo em camundongos obesos e diabéticos . Nat Med 2017 ; 23 : 107 - 13 .
- 18 , , , , , et al . O receptor P2X7 medeia a secreção de IL-1 β dependente de NLRP3 e a proliferação do parasita em células epiteliais do intestino delgado humano infectadas com Toxoplasma gondii . Parasit Vectors 2018 ; 11 : 1 .
- 19 , , , , , et al . O inflamassoma NLRP6 orquestra a interface microbiana-hospedeiro do cólon regulando a secreção de muco das células caliciformes . Cell 2014 ; 156 : 1045 - 59 .
- 20 , , , , , et al . O inflamassoma Nlrp9b restringe a infecção por rotavírus nas células epiteliais intestinais . Nature 2017 ; 546 : 667 - 70 .
- 21 , , . A expressão de NLRC4 em células epiteliais intestinais medeia a proteção contra um patógeno entérico . Mucosal Immunol 2014 ; 7 : 775 - 85 .
- 22 , , , , , et al . Os inflamassomas NAIP-NLRC4 coordenam a expulsão de células epiteliais intestinais com eicosanóide e liberação de IL-18 via ativação de Caspase-1 e -8 . Immunity 2017 ; 46 : 649 - 59 .
- 23 , , , , , et al . As células de Paneth secretam lisozima via autofagia secretora durante a infecção bacteriana do intestino . Science 2017 ; 357 : 1047 - 52 .
- 24 , , , , , et al . Os metabólitos bacterianos simbióticos regulam a função da barreira gastrointestinal por meio do sensor xenobiótico PXR e do receptor Toll-like 4 . Immunity 2014 ; 41 : 296 - 310 .
- 25 , , , , , et al . Catabólitos de triptofano da microbiota envolvem o receptor de hidrocarboneto de arila e equilibram a reatividade da mucosa via interleucina-22 . Immunity 2013 ; 39 : 372 - 85 .
- 26 , , , , , et al . O sensor ambiental AHR protege contra danos inflamatórios, mantendo a homeostase das células-tronco intestinais e a integridade da barreira . Immunity 2018 ; 49 : 353 - 62 e5.
- 27 , , , , , et al . O ácido indoleacrílico produzido por espécies de peptostreptococos comensais suprime a inflamação . Cell Host Microbe 2017 ; 22 : 25 - 37 e6.
- 28 , , , , , et al . Promoção da renovação das células epiteliais intestinais por bactérias comensais: papel dos ácidos graxos de cadeia curta . PLoS One 2016 ; 11 : e0156334.
- 29 , , , , , et al . O butirato de origem microbiana promove a função de barreira epitelial por meio da repressão da claudina-2 dependente do receptor de IL-10 . J Immunol 2017 ; 199 : 2976 - 84 .
- 30 , , , , , et al . Os receptores sensíveis a metabólitos GPR43 e GPR109A facilitam a homeostase intestinal induzida por fibra alimentar por meio da regulação do inflamassoma . Nat Commun 2015 ; 6 : 6734 .
- 31 , , , , , et al . A conversa cruzada entre os ácidos graxos de cadeia curta derivados da microbiota e o HIF epitelial intestinal aumenta a função de barreira do tecido . Cell Host Microbe 2015 ; 17 : 662 - 71 .
- 32 , . Microbiota intestinal, metabólitos e imunidade do hospedeiro . Nat Rev Immunol 2016 ; 16 : 341 - 52 .
- 33 , , , , , et al . GPR43 medeia a regulação de SCFA do metabólito da microbiota da expressão de peptídeos antimicrobianos em células epiteliais intestinais via ativação de mTOR e STAT3 . Mucosal Immunol 2018 ; 11 : 752 - 62 .
- 34 , , , , . As células epiteliais intestinais e o microbioma são reprogramados rapidamente no início da infecção por Citrobacter rodentium do cólon . MBio 2019 ; 10 : e00062-19.
- 35 , , , , , et al . Uma população de células enterocromafins epiteliais do intestino é mecanossensível e requer Piezo2 para converter a força em liberação de serotonina . Proc Natl Acad Sci USA 2018 ; 115 : E7632 - 41 .
- 36 , . Mecanismos serotonérgicos que regulam o trato GI: evidências experimentais e relevância terapêutica . Handb Exp Pharmacol 2017 ; 239 : 319 - 42 .
- 37 , , , , , et al . Bactérias indígenas da microbiota intestinal regulam a biossíntese de serotonina do hospedeiro . Cell 2015 ; 161 : 264 - 76 .
- 38 , , , , , et al . A expressão elevada de amiloide A 3 sérico protege o epitélio do cólon contra lesão aguda por meio da indução dependente de TLR2 da expressão de IL-22 de neutrófilos em um modelo de colite em camundongo . Front Immunol 2018 ; 9 : 1503 .
- 39 , , , , , et al . Um circuito ILC2 de célula-tufo desencadeada por metabólitos conduz a remodelação do intestino delgado . Cell 2018 ; 174 : 271 - 84 e14.
- 40 , , , , , et al . Função essencial independente de autofagossomo para a proteína autofágica Atg5 na imunidade celular a patógenos intracelulares . Cell Host Microbe 2008 ; 4 : 458 - 69 .
- 41 , , , , , et al . A autofagia protege contra a tuberculose ativa, suprimindo a carga bacteriana e a inflamação . Proc Natl Acad Sci USA 2012 ; 109 : E3168 - 76 .
- 42 , , , . O DNA da tuberculose tem como alvo as bactérias para autofagia, ativando a via de detecção do DNA do hospedeiro . Cell 2012 ; 150 : 803 - 15 .
- 43 , , , , , et al . Atg16l1 é necessário para autofagia em células epiteliais intestinais e proteção de camundongos contra infecção por Salmonella . Gastroenterology 2013 ; 145 : 1347 - 57 .
- 44 , , , . A autofagia epitelial intestinal é essencial para a defesa do hospedeiro contra bactérias invasivas . Cell Host Microbe 2013 ; 13 : 723 - 34 .
- 45 , , , , , et al . A autofagia prejudicada nas células epiteliais intestinais altera a microbiota intestinal e as respostas imunes do hospedeiro . Appl Environ Microbiol 2018 ; 84 : e00880-18.
- 46 , , , , , et al . A modulação da composição da microbiota intestinal pela sinalização da serotonina influencia a resposta imune intestinal e a suscetibilidade à colite . Cell Mol Gastroenterol Hepatol 2019 ; 7 : 709 - 28 .
- 47 , , . Peptídeos antimicrobianos intestinais durante a homeostase, infecção e doença . Front Immunol 2012 ; 3 : 310 .
- 48 , . Células Paneth, peptídeos antimicrobianos e manutenção da homeostase intestinal . Nat Rev Microbiol 2011 ; 9 : 356 - 68 .
- 49 , , , , , et al . As defensinas entéricas são reguladores essenciais da ecologia microbiana intestinal . Nat Immunol 2010 ; 11 : 76 - 83 .
- 50 , , , , , et al . O inflamassoma NLRP6 regula a ecologia microbiana do cólon e o risco de colite . Cell 2011 ; 145 : 745 - 57 .
- 51 , , , , , et al . Os metabólitos modulados pela microbiota moldam o microambiente intestinal ao regular a sinalização do inflamassoma NLRP6 . Cell 2015 ; 163 : 1428 - 43 .
- 52 , , , , , et al . Os inflamassomas dependentes de Nlrp6 e ASC não moldam a composição da microbiota intestinal comensal . Immunity 2017 ; 47 : 339 - 48 e4.
- 53 , , , , , et al . A proteína NLR NLRP6 não afeta a composição da microbiota intestinal . Cell Rep 2017 ; 21 : 3653 - 61 .
- 54 , . Contabilizando as interações hospedeiro-microbioma recíprocas na ciência experimental . Nature 2016 ; 534 : 191 - 9 .
- 55 , , , , , et al . A sinalização Nod1 e Nod2 não altera a composição das comunidades bacterianas intestinais na homeostase . Gut Microbes 2013 ; 4 : 222 - 31 de .
- 56 , , , , . O sensor bacteriano Nod2 evita a inflamação do intestino delgado ao restringir a expansão do Bacteroides vulgatus comensal . Immunity 2014 ; 41 : 311 - 24 .
- 57 , , , , , et al . Comparação de métodos de co-alojamento e ninhada para padronização da microbiota em modelos de camundongos . Cell Rep 2019 ; 27 : 1910 - 9 e2.
- 58 , , , , , et al . O receptor 4 epitelial intestinal tipo Toll previne a síndrome metabólica ao regular as interações entre os micróbios e as células epiteliais intestinais em camundongos . Mucosal Immunol 2018 ; 11 : 727 - 40 .
- 59 , . A mecanosensificação regula a virulência em Escherichia coli O157: H7 . Gut Microbes 2016 ; 7 : 63 - 7 .
- 60 , , , , , et al . O hospedeiro molda a microbiota intestinal por meio de MicroRNA fecal . Cell Host Microbe 2016 ; 19 : 32 - 43 .
- 61 , , , , , . Bactérias simbióticas do intestino humano com prioridades metabólicas variáveis para glicanos da mucosa do hospedeiro . MBio 2015 ; 6 : e01282-15.
- 62 , , , , . Degradação microbiana de carboidratos complexos no intestino . Gut Microbes 2012 ; 3 : 289 - 306 .
- 63 , , . Glicosilação epitelial na homeostase intestinal e inflamação . Nat Immunol 2016 ; 17 : 1244 - 51 .
- 64 , , , , , et al . Desvendando a especificidade e o mecanismo de reconhecimento do ácido siálico pelo simbionte intestinal Ruminococcus gnavus . Nat Commun 2017 ; 8 : 2196 .
- 65 , , . TGF- β na doença inflamatória intestinal: um regulador chave das células imunológicas, do epitélio e da microbiota intestinal . J Gastroenterol 2017 ; 52 : 777 - 87 .
- 66 , , . Linfopoietina estromal tímica: para encurtar uma longa história . Cell Mol Gastroenterol Hepatol 2017 ; 3 : 174 - 82 .
- 67 , , . Impacto do ácido retinóico nas células do sistema imunológico e doenças inflamatórias . Mediators Inflamm 2018 ; 2018 : 3067126 .
- 68 , , . Ajuste de citocinas da função epitelial intestinal . Front Immunol 2018 ; 9 : 1270 .
- 69 , , , , , , et al . A IL-15 epitelial é um regulador crítico da motilidade dos linfócitos intraepiteliais γδ na mucosa intestinal . J Immunol 2018 ; 201 : 747 - 56 .
- 70 , , , , , et al . Os linfócitos intraepiteliais γδ são mediadores essenciais da homeostase microbiana do hospedeiro na superfície da mucosa intestinal . Proc Natl Acad Sci USA 2011 ; 108 : 8743 - 8 .
- 71 , , , , , . O crosstalk das células T epitelial intestinal e intraepitelial medeia uma resposta dinâmica à infecção . Cell 2017 ; 171 : 783 - 94 e13.
- 72 , , , , , et al . Indução de células Th17 por adesão de micróbios às células epiteliais intestinais . Cell 2015 ; 163 : 367 - 80 .
- 73 , , , , , et al . Um circuito IL-23R / IL-22 regula a amilóide A do soro epitelial para promover respostas Th17 efetoras locais . Cell 2015 ; 163 : 381 - 93 .
- 74 , , , , , et al . A endocitose de antígenos comensais pelas células epiteliais intestinais regula a homeostase das células T da mucosa . Science 2019 ; 363 : eaat4042 .
- 75 , , , , , et al . O receptor do ácido retinóico epitelial β regula soro amilóide A expressão e dependente de vitamina A imunidade intestinal . Proc Natl Acad Sci USA 2019 ; 116 : 10911 - 6 .
- 76 , , , , , et al . Células epiteliais intestinais sintetizar glucocorticóides e regular a activação das células T . J Exp Med 2004 ; 200 : 1635 - 46 .
- 77 , , , , , et al . A síntese de glicocorticóides mediada por LRH-1 em enterócitos protege contra doença inflamatória intestinal . Proc Natl Acad Sci USA 2007 ; 104 : 13098 - 103 .
- 78 , , , , . Efeitos da sensibilidade alterada glucocorticóide na linhagem de células T em timócitos e células T homeostase . FASEB J 2002 ; 16 : 727 - 9 .
- 79 , , , , , et al . As células T reguladoras Foxp3 + deficientes do receptor de glicocorticóide falham em controlar a doença inflamatória intestinal experimental . Front Immunol 2019 ; 10 : 472 .
- 80 , , , , , et al . Dímeros do receptor de glicocorticóide controlam a inflamação intestinal induzida por STAT1 e TNF em camundongos . J Clin Invest 2018 ; 128 : 3265 - 79 .
- 81 , , . A serotonina fornece um sinal acessório para aumentar a ativação das células T, sinalizando por meio do receptor 5-HT7 . Blood 2007 ; 109 : 3139 - 46 .
- 82 , , , , , et al . Regulação do tráfego induzido pela serotonina e migração de eosinófilos . PLoS One 2013 ; 8 : e54840.
- 83 , , , . A ativação do receptor da serotonina 5-HT2A bloqueia a inflamação mediada pelo TNF- α in vivo . PLoS One 2013 ; 8 : e75426.
- 84 , , , , , . A amostragem de antígenos pelas células M intestinais é a principal via de iniciação da produção de IgA na mucosa para bactérias entéricas comensais . Mucosal Immunol 2016 ; 9 : 907 - 16 .
- 85 , , , , , et al . As células caliciformes entregam antígeno luminal às células dendríticas CD103 + no intestino delgado . Nature 2012 ; 483 : 345 - 9 .
- 86 , , , , . A detecção microbiana por células caliciformes controla a vigilância imunológica de antígenos luminais no cólon . Mucosal Immunol 2015 ; 8 : 198 - 210 .
- 87 , , , , , et al . O encontro de antígenos microbianos durante um intervalo de pré-desmame é crítico para a tolerância às bactérias intestinais . Sci Immunol 2017 ; 2 .
- 88 , , , , , et al . As passagens de antígenos associados às células caliciformes são inibidas durante a infecção por Salmonella typhimurium para prevenir a disseminação do patógeno e limitar as respostas aos antígenos dietéticos . Mucosal Immunol 2018 ; 11 : 1103 - 13 .
- 89 , , , , , et al . Imunidade protetora da mucosa mediada por CD1d epitelial e IL-10 . Nature 2014 ; 509 : 497 - 502 .
- 90 , , . As células epiteliais do intestino delgado humano expressam constitutivamente os elementos-chave para o processamento de antígenos e a produção de exossomos . Blood Cells Mol Dis 2005 ; 35 : 122 - 8 .
- 91 , , , , , et al . O interferon- γ induz uma mudança do fenótipo da superfície celular nas células epiteliais intestinais T84 . Am J Physiol 1994 ; 267 : C402 - 10 .
- 92 , , , , , et al . As doenças inflamatórias intestinais influenciam os principais compartimentos do complexo de histocompatibilidade classe I (MHC I) e II nas células epiteliais intestinais . Clin Exp Immunol 2013 ; 172 : 280 - 9 .
- 93 , , , , , . As células epiteliais intestinais de pacientes com doença inflamatória intestinal estimulam preferencialmente as células T CD4 + a proliferar e secretar interferon- γ . Am J Physiol Gastrointest Liver Physiol 2007 ; 292 : G1630 - 40 .
- 94 , , , , , et al . Expansão de células T regulatórias CD4 + Foxp3 + induzida por interação dirigida por antígeno com células epiteliais intestinais independentes de células dendríticas locais . Gut 2009 ; 58 : 211 - 9 .
- 95 , , , , , et al . O interferon- γ induz a expressão de MHC classe II nas células epiteliais intestinais e protege os camundongos da colite . PLoS One 2014 ; 9 : e86844.
- 96 , , , , , et al . A interleucina-22 promove a regeneração epitelial mediada por células-tronco intestinais . Nature 2015 ; 528 : 560 - 4 .
- 97 , , , , , et al . Uma rede de citocinas envolvendo IL-36 γ , IL-23 e IL-22 promove a defesa antimicrobiana e a recuperação do dano à barreira intestinal . Proc Natl Acad Sci USA 2018 ; 115 : E5076 - 85 .
- 98 , , , , , et al . A interleucina-22 previne a disbiose microbiana e promove a regeneração da barreira intestinal após lesão aguda . Shock 2017 ; 48 : 657 - 65 .
- 99 , , , , , et al . As células linfoides inatas regulam a glicosilação das células epiteliais intestinais . Science 2014 ; 345 : 1254009 .
- 100 , , , , , et al . IL-22 melhora a inflamação intestinal em um modelo de colite ulcerosa em camundongo . J Clin Invest 2008 ; 118 : 534 - 44 .
- 101 , , , , , et al . IL-22 regula positivamente a claudina-2 epitelial para conduzir a diarreia e a depuração de patógenos entéricos . Cell Host Microbe 2017 ; 21 : 671 - 81 e4.
- 102 , , , , , et al . As células do tufo epitelial intestinal iniciam a imunidade mucosa tipo 2 aos helmintos parasitas . Nature 2016 ; 529 : 226 - 30 .
- 103 , , , , , et al . IL-33, IL-25 e TSLP induzem um perfil fenotípico e de ativação distinto em células linfóides inatas tipo 2 humanas . Blood Adv 2017 ; 1 : 577 - 89 .
- 104 , , , , , et al . RELM β / FIZZ2 é uma molécula imunoefetora específica para células caliciformes no trato gastrointestinal . Proc Natl Acad Sci USA 2004 ; 101 : 13596 - 600 .
- 105 , , , , , et al . A interleucina-22 medeia a defesa inicial do hospedeiro contra a adesão e eliminação de patógenos bacterianos . Nat Med 2008 ; 14 : 282 - 9 .
- 106 , , , , . IL-17a e IL-22 induzem a expressão de antimicrobianos em células epiteliais gastrointestinais e podem contribuir para a defesa das células epiteliais contra o Helicobacter pylori . PLoS One 2016 ; 11 : e0148514.
- 107 , , , , , et al . Papéis diferenciais para interleucina-23 e interleucina-17 na imunorregulação intestinal . Immunity 2015 ; 43 : 739 - 50 .
- 108 , , , , , et al . A produção de IL-17 independente de interleucina 23 regula a permeabilidade epitelial intestinal . Immunity 2015 ; 43 : 727 - 38 .
- 109 , , , , , et al . O fator de crescimento FGF2 coopera com a interleucina-17 para reparar o dano epitelial intestinal . Immunity 2015 ; 43 : 488 - 501 .
- 110 , , , , , et al . A sinalização do receptor de TNF epitelial promove o reparo da mucosa na doença inflamatória intestinal . J Immunol 2017 ; 199 : 1886 - 97 .
- 111 , , , , , . O papel dos macrófagos dependentes de CSF1R no controle do nicho de células-tronco intestinais . Nat Commun 2018 ; 9 : 1272 .
- 112 , , , , , et al . A IL-10 derivada de macrófagos medeia o reparo da mucosa por sinalização epitelial WISP-1 . J Clin Invest 2017 ; 127 : 3510 - 20 .
- 113 , , , , , et al . A sinalização de TGF- β em células dendríticas governa a homeostase colônica controlando a diferenciação epitelial e a microbiota luminal . J Immunol 2016 ; 196 : 4603 - 13 .
- 114 , , , , , et al . Caracterização morfológica e funcional da cadeia β 2 do IL-12R em células epiteliais intestinais: implicações para a imunorregulação local e sistêmica . Front Immunol 2018 ; 9 : 1177 .
- 115 , , , , , et al . Identificação de espécies de bactérias simbiontes do intestino humano que, por si só, podem induzir células Th17 intestinais em camundongos . Proc Natl Acad Sci USA 2016 ; 113 : E8141 - 50 .
- 116 , , , , , et al . Os metabólitos microbianos, ácidos graxos de cadeia curta, regulam a homeostase das células Treg do cólon . Science 2013 ; 341 : 569 - 73 .
- 117 , , , , , et al . Indução de Treg por uma mistura racionalmente selecionada de cepas de Clostridia da microbiota humana . Nature 2013 ; 500 : 232 - 6 .
- 118 , , , , , et al . Os metabólitos produzidos por bactérias comensais promovem a geração de células T regulatórias periféricas . Nature 2013 ; 504 : 451 - 5 .
- 119 , , , , , et al . Geração rápida e eficiente de células T reguladoras para antígenos comensais na periferia . Cell Rep 2016 ; 17 : 206 - 20 .
- 120 , , , , , et al . Uma reação de desmame à microbiota é necessária para a resistência a imunopatologias no adulto . Immunity 2019 ; 50 : 1276 - 88 e5.
- 121 , , , , , et al . As células T regulatórias dependentes de c-MAF medeiam a tolerância imunológica a um patobionte intestinal . Nature 2018 ; 554 : 373 - 7 .
- 122 , , , , , et al . Um grande polissacarídeo produzido pelo Helicobacter hepaticus induz uma assinatura de um gene antiinflamatório em macrófagos . Cell Host Microbe 2017 ; 22 : 733 - 45 e5.
- 123 , , , , , et al . As espécies de Helicobacter são impulsionadores potentes das respostas das células T colônicas na homeostase e na inflamação . Sci Immunol 2017 ; 2 .
- 124 , , , , , et al . Helicobacter bilis desencadeia reatividade imunológica persistente a antígenos derivados de bactérias comensais em camundongos C3H / HeN gnotobióticos . Gut 2007 ; 56 : 934 - 40 .
- 125 , , , , , et al . Os metabólitos do ácido biliar controlam a diferenciação das células Th17 e Treg . bioRxiv 2018 ; 465344 .https://doi.org/10.1101/465344
- 126 , , , . Expansão de linfócitos intraepiteliais intestinais com receptor de células T αβ após colonização microbiana em camundongos livres de germe e sua independência do timo . Immunology 1993 ; 79 : 32 - 7 .
- 127 , , , , . Recrutamento proliferativo de linfócitos intraepiteliais intestinais após colonização microbiana de camundongos livres de germes . Eur J Immunol 1996 ; 26 : 945 - 8 .
- 128 , , , , , et al . Desenvolvimento e função citolítica de linfócitos T intraepiteliais intestinais em camundongos com antígeno minimizado . Immunology 1996 ; 89 : 268 - 73 .
- 129 , , , , , et al . Lactobacillus reuteri induz células T CD4 + CD8 αα + intraepiteliais intestinais . Science 2017 ; 357 : 806 - 10 .
- 130 , , , , , et al . A adaptação tecidual de células T CD4 + regulatórias e intraepiteliais controla a inflamação intestinal . Science 2016 ; 352 : 1581 - 6 .
- 131 , , , , . A imunidade adaptativa do hospedeiro altera a microbiota intestinal . ISME J 2015 ; 9 : 770 - 81 .
- 132 , , , , , et al . As células T CD4 + convencionais regulam as células linfóides inatas intestinais produtoras de IL-22 . Mucosal Immunol 2014 ; 7 : 1045 - 57 .
- 133 , , , , , et al . Os camundongos BALB / ce C57BL / 6 diferem na abundância de IgA polirreativa, o que impacta a geração de IgA antígeno-específico e diversidade da microbiota . Immunity 2015 ; 43 : 527 - 40 .
- 134 , , , , , et al . A microbiota intestinal utiliza imunoglobulina A para colonização da mucosa . Science 2018 ; 360 : 795 - 800 .
- 135 , , , , , et al . IgG anti-comensal conduz a inflamação intestinal e imunidade tipo 17 na colite ulcerosa . Immunity 2019 ; 50 : 1099 - 114 e10.
- 136 , , , , , et al . As células T Foxp3 + regulam a seleção da imunoglobulina e facilitam a diversificação das espécies bacterianas responsáveis pela homeostase imunológica . Immunity 2014 ; 41 : 152 - 65 .
- 137 , , , , , et al . As células T regulatórias geradas extratimicamente estabelecem um nicho para bactérias que vivem na fronteira intestinal e afetam o equilíbrio fisiológico dos metabólitos . Immunity 2018 ; 48 : 1245 - 57 e9.
- 138 , , . A imunidade adaptativa aumenta o ritmo e a previsibilidade da mudança evolutiva nas bactérias do intestino comensal . Nat Commun 2015 ; 6 : 8945 .
- 139 , , , . Integridade epitelial, morte celular e perda celular no intestino delgado de mamíferos . Histol Histopathol 1999 ; 14 : 257 - 67 .
- 140 , , , , , et al . O TLR9 limita as respostas antimicrobianas entéricas e promove a resistência à colonização baseada na microbiota durante a infecção por Citrobacter rodentium . Cell Microbiol 2019 ; 21 : e13026.
- 141 , , , , , et al . TLR9 regula a via NF- κ B-NLRP3-IL-1 β negativamente na inflamação intestinal mediada por NKG2D induzida por salmonela . J Immunol 2017 ; 199 : 761 - 73 .
- 142 , , , , , et al . As cepas patogênicas de Helicobacter pylori translocam o DNA e ativam o TLR9 por meio do sistema de secreção cag tipo IV associado ao câncer . Oncogene 2016 ; 35 : 6262 - 9 .
- 143 , , , , , et al . Um receptor toll-like reconhece o DNA bacteriano . Nature 2000 ; 408 : 740 - 5 .
- 144 , , , , , et al . A apoptose de células epiteliais intestinais restringe a infecção por Clostridium difficile em um modelo de colite pseudomembranosa . Nat Commun 2018 ; 9 : 4846 .
- 145 , , , , , et al . Os receptores de inflamassoma NLRC4 para flagelina bacteriana e aparelho de secreção do tipo III . Nature 2011 ; 477 : 596 - 600 .
- 146 , , , , , . O TLR4 liga a imunidade inata e a resistência à insulina induzida por ácidos graxos . J Clin Invest 2006 ; 116 : 3015 - 25 .
- 147 , , , , , et al . Os ácidos graxos e os eicosanóides regulam a expressão gênica por meio de interações diretas com os receptores α e γ ativados por proliferadores de peroxissoma . Proc Natl Acad Sci USA 1997 ; 94 : 4318 - 23 de .
- 148 , , , , , et al . Papel crítico para a mobilização de cálcio na ativação do inflamassoma NLRP3 . Proc Natl Acad Sci USA 2012 ; 109 : 11282 - 7 .
- 149 , , , , , et al . Produção alterada de citocinas em camundongos sem receptores P2X (7) . J Biol Chem 2001 ; 276 : 125 - 32 .
- 150 , , , , . Os ácidos graxos de cadeia curta ativam GPR41 e GPR43 nas células epiteliais intestinais para promover respostas inflamatórias em camundongos . Gastroenterology 2013 ; 145 : 396 - 406 e1–10.
- 151 , , , , , et al . Os ácidos graxos de cadeia curta derivados da dieta estimulam as células epiteliais intestinais a induzir células dendríticas tolerogênicas da mucosa . J Immunol 2017 ; 198 : 2172 - 81 .
- 152 , , , . Da fibra dietética à fisiologia do hospedeiro: ácidos graxos de cadeia curta como metabólitos bacterianos essenciais . Cell 2016 ; 165 : 1332 - 45 .
- 153 , , . A autofagia de células epiteliais intestinais é necessária para proteger contra a apoptose induzida por TNF durante a colite crônica em camundongos . Cell Host Microbe 2018 ; 23 : 191 - 202 e4.
- 154 , , , , , et al . A proteína autofágica ATG16L1 previne a necroptose no epitélio intestinal . J Exp Med 2017 ; 214 : 3687 - 705 .
- 155 . Autofagia bacteriana: ataque e defesa na interface patógeno-hospedeiro . Cell Mol Gastroenterol Hepatol 2017 ; 4 : 237 - 43 .
- 156 , , , , , et al . Explorar uma interação hospedeiro-comensal para promover a função de barreira intestinal e a tolerância a patógenos entéricos . Sci Immunol 2016 ; 1 : eaai7732 .
- 157 , , , , , et al . Reconhecimento do hospedeiro de dipeptídeo muramil bacteriano mediado por NOD2. implicações para a doença de Crohn . J Biol Chem 2003 ; 278 : 5509 - 12 .
- 158 , , , , , et al . O antígeno A secretado de Enterococcus faecium gera muropeptídeos para aumentar a imunidade do hospedeiro e limitar a patogênese bacteriana . Elife 2019 ; 8 .
- 159 , , , , , et al . O receptor do pregnano X regula a inflamação induzida pelo patógeno e a defesa do hospedeiro contra uma infecção bacteriana intracelular por meio do receptor toll-like 4 . Sci Rep 2016 ; 6 : 31936 .
Citando literatura
Número de vezes citado de acordo com CrossRef: 39
- Yu-Huan Chen, Jenn-Yeu Shin, Hsiu-Mei Wei, Chi-Chien Lin, Linda CH Yu, Wei-Ting Liao, Dz-Chi Chen, Ching-Liang Chu, Prevenção de colite de camundongo induzida por sulfato de dextrana e sódio por proteína fúngica Ling Zhi-8 via promoção da função de barreira das células epiteliais intestinais , Food & Function , 10.1039 / D0FO02604B , 12 , 4 , (1639-1650) , (2021) .
- Mi-Young Kim, Sang-Woon Choi, modulação dietética da microbiota intestinal para o alívio da síndrome do intestino irritável , Nutrition Research and Practice , 10.4162 / nrp.2021.15.4.411 , 15 , 4 , (411) , (2021) .
- Wenting Hong, Dongke Xu, Xiaowei Song, Baolin Niu, Ziyan Zhuang, Yiteng Lu, Xiaohong Lei, Runjun Ma, Chao Lu, Ning Sun, Yimin Mao, Xiaobo Li, vitamina A e ácido retinóico aceleram a atenuação da adaptabilidade intestinal após a alimentação induzida por dieta rica em gordura em ratos , The Journal of Nutritional Biochemistry , 10.1016 / j.jnutbio.2021.108803 , (108803) , (2021) .
- Chang H. Kim, Controle de funções de linfócitos por ácidos graxos de cadeia curta derivados da microbiota intestinal , Cellular & Molecular Immunology , 10.1038 / s41423-020-00625-0 , 18 , 5 , (1161-1171) , (2021) .
- Ai-Ru Liu, Shao-Peng Yang, Xiao-Lan Zhang, Efeitos da interação entre células-tronco mesenquimais e microbiota intestinal no tratamento de doença inflamatória intestinal , World Chinese Journal of Digestology , 10.11569 / wcjd.v29.i6.312 , 29 , 6 , (312-318) , (2021) .
- Julia Álvarez, José Manuel Fernández Real, Francisco Guarner, Miguel Gueimonde, Juan Miguel Rodríguez, Miguel Saenz de Pipaon, Yolanda Sanz, Microbiota intestinal y salud , Gastroenterología y Hepatología , 10.1016 / j.gastrohep.2021.01.009 , (2021) .
- Sigita Malijauskaite, Sinead Connolly, David Newport, Kieran McGourty, Gradientes no compartimento de células-tronco intestinais in vivo e sua recapitulação in vitro em plataformas miméticas , Cytokine & Growth Factor Reviews , 10.1016 / j.cytogfr.2021.03.002 , (2021) .
- David Fawkner-Corbett, Agne Antanaviciute, Kaushal Parikh, Marta Jagielowicz, Ana Sousa Gerós, Tarun Gupta, Neil Ashley, Doran Khamis, Darren Fowler, Edward Morrissey, Chris Cunningham, Paul RV Johnson, Hashem Koohy, Alison Simmons, análise espacial temporal humana desenvolvimento intestinal em resolução de célula única , Cell , 10.1016 / j.cell.2020.12.016 , 184 , 3 , (810-826.e23) , (2021) .
- Julia Álvarez, José Manuel Fernández Real, Francisco Guarner, Miguel Gueimonde, Juan Miguel Rodríguez, Miguel Saenz de Pipaon, Yolanda Sanz, Micróbios intestinais e saúde , Gastroenterología y Hepatología (Edição em Inglês) , 10.1016 / j.gastre.2021.01.002 , ( 2021) .
- David A Constant, Timothy J Nice, Isabella Rauch, Sensing imunológico inato por barreiras epiteliais , Current Opinion in Immunology , 10.1016 / j.coi.2021.07.014 , 73 , (1-8) , (2021) .
- Zsolt I. Komlósi, Willem van de Veen, Nóra Kovács, Gergő Szűcs, Milena Sokolowska, Liam O'Mahony, Mübeccel Akdis, Cezmi A. Akdis, Mecanismos celulares e moleculares da asma alérgica , Aspectos moleculares da medicina , 10.1016 / j.mam .2021.100995 , (100995) , (2021) .
- Mats Bemark, Davide Angeletti, Conheça seu inimigo ou encontre seu amigo? —Induction of IgA at mucosal surface , Immunological Reviews , 10.1111 / imr.13014 , 303 , 1 , (83-102) , (2021) .
- Ziteng Deng, Deping Han, Yuying Wang, Qiuzhen Wang, Xue Yan, Shujing Wang, Xuelian Liu, Weiping Song, Yunfei Ma, Lactobacillus casei protege a mucosa intestinal de danos em pintinhos causados por Salmonella pullorum através da regulação da imunidade e da via de sinalização Wnt e manutenção a abundância de microbiota intestinal , Poultry Science , 10.1016 / j.psj.2021.101283 , (101283) , (2021) .
- Saima Rehman, Adnan H. Gora, Prabhugouda Siriyappagouder, Sylvia Brugman, Jorge MO Fernandes, Jorge Dias, Viswanath Kiron, transcriptoma intestinal de peixe-zebra destaca respostas inflamatórias moderadas à soja dietética e eficácia de β-glucano de levedura , Journal of Fish Diseases , 10.1111 / jfd.13484 , 44 , 10 , (1619-1637) , (2021) .
- Karin Enderle, Martin Dinkel, Eva-Maria Spath, Benjamin Schmid, Sebastian Zundler, Philipp Tripal, Markus F. Neurath, Kai Hildner, Clemens Neufert, Dynamic Imaging of IEL-IEC Co-Cultures Permite Quantificação da Migração de Células T CD103-Dependentes , International Journal of Molecular Sciences , 10.3390 / ijms22105148 , 22 , 10 , (5148) , (2021) .
- Laura Ailioaie, Gerhard Litscher, Probiotics, Photobiomodulation, and Disease Management: Controversies and Challenges , International Journal of Molecular Sciences , 10.3390 / ijms22094942 , 22 , 9 , (4942) , (2021) .
- Thaísa Agrizzi Verediano, Hércia Stampini Duarte Martino, Maria Cristina Dias Paes, Elad Tako, Efeitos da Antocianina na Saúde Intestinal: Uma Revisão Sistemática , Nutrientes , 10.3390 / nu13041331 , 13 , 4 , (1331) , (2021) .
- Xiaoyan Wang, Qian Yang, Xiaofeng Zhou, Ting Chen, Liwen Dou, Furong Wang, Wei Wang, Shenling Baizhu Powder inhibits RV-SA11-Induced Inflammation and Rotavirus Enteritis via TLR4 / MyD88 / NF-κB Signaling Pathway , Frontiers in Pharmacology , 10.3389 /fphar.2021.642685 , 12 , (2021) .
- Julio Villena, Chang Li, Maria Guadalupe Vizoso-Pinto, Jacinto Sacur, Linzhu Ren, Haruki Kitazawa, Lactiplantibacillus plantarum como um adjuvante potencial e sistema de entrega para o desenvolvimento de SARS-CoV-2 Vacinas orais , Microorganismos , 10.3390 / microorganismos9040683 , 9 , 4 , (683) , (2021) .
- María Ángeles Martín, Sonia Ramos, Impact of Dietary Flavanols on Microbiota, Imunity and Inflammation in Metabolic Diseases , Nutrients , 10.3390 / nu13030850 , 13 , 3 , (850) , (2021) .
- Lingling Huang, Chanisa Thonusin, Nipon Chattipakorn, Siriporn C. Chattipakorn, Impacts of gut microbiota on gestational diabetes mellitus: a abrangente review , European Journal of Nutrition , 10.1007 / s00394-021-02483-6 , (2021) .
- Xiang-Guang Li, Ming-xia Chen, Su-qing Zhao, Xiu-qi Wang, Intestinal Models for Personalized Medicine: from Conventional Models to Microfluidic Primary Intestine-on-a-chip , Stem Cell Reviews and Reports , 10.1007 / s12015- 021-10205-y , (2021) .
- Dan Qiao, Ziwei Zhang, Yali Zhang, Qian Chen, Yujun Chen, Yingjue Tang, Xiong Sun, Zhipeng Tang, Yancheng Dai, Regulação da Autofagia de Estresse do Retículo Endoplasmático: Um Alvo Terapêutico Potencial para Colite Ulcerativa , Fronteiras em Farmacologia , 10.3389 / fphar .2021.697360 , 12 , (2021) .
- Roberta Saleri, Paolo Borghetti, Francesca Ravanetti, Melania Andrani, Valeria Cavalli, Elena De Angelis, Luca Ferrari, Paolo Martelli, Um modelo de co-cultura de IPEC-J2 e PBMC de suínos para estudar a capacidade de resposta das células epiteliais intestinais: o efeito regulador de Arginina Privação , Animais , 10.3390 / ani11092756 , 11 , 9 , (2756) , (2021) .
- Jane A. Foster, Glen B. Baker, Serdar M. Dursun, The Relationship Between the Gut Microbiome-Immune System-Brain Axis and Major Depressive Disorder , Frontiers in Neurology , 10.3389 / fneur.2021.721126 , 12 , (2021) .
- Jinze Li, Qiuke Li, Nan Gao, Zhihua Wang, Feng Li, Jianping Li, Anshan Shan, exopolissacarídeos produzidos por Lactobacillus rhamnosus GG aliviam dano oxidativo intestinal induzido por peróxido de hidrogênio e apoptose através das vias Keap1 / Nrf2 e Bax / Bcl-2 em vitro , Food & Function , 10.1039 / D1FO00277E , (2021) .
- Dongjia Lin, Lisa Yang, Liling Wen, Huanzi Lu, Qianming Chen, Zhi Wang, Conversa cruzada entre a microbiota oral, imunidade da mucosa e a barreira epitelial regula a patogênese da doença da mucosa oral , Imunologia da mucosa , 10.1038 / s41385-021-00413-7 , (2021) .
- Cezmi A. Akdis, A hipótese da barreira epitelial explica o aumento da alergia, autoimunidade e outras condições crônicas? , Nature Reviews Immunology , 10.1038 / s41577-021-00538-7 , (2021) .
- Qing Wang, Yuqi Luo, K Ray Chaudhuri, Richard Reynolds, Eng-King Tan, Sven Pettersson, O papel da disbiose intestinal na doença de Parkinson: insights mecanicistas e opções terapêuticas , Brain , 10.1093 / brain / awab156 , (2021) .
- Shiqiong Wang, Suiliang Zhu, Jingjing Zhang, Haiyan Li, Dongji Yang, Shucheng Huang, Zhanyong Wei, Xiuli Liang, Zhixiang Wang, A suplementação com cultura de levedura melhora a integridade das proteínas de junção intestinal através da via NOD1 / NF ‐ κB P65 em leitões desmamados e células IPEC-J2 desafiadas com H2O2 , Journal of Functional Foods , 10.1016 / j.jff.2020.104058 , 72 , (104058) , (2020) .
- Sonia Ramos, María Ángeles Martín, Impact of diet on gut microbiota , Current Opinion in Food Science , 10.1016 / j.cofs.2020.09.006 , (2020) .
- Muhammad Shahid Riaz Rajoka, Hafiza Mahreen Mehwish, Yongai Xiong, Xun Song, Nazim Hussain, Qinchang Zhu, Zhendan He , Nanomedicina direcionada à microbiota intestinal para terapia do câncer: Desafios e considerações futuras , Tendências em Ciência e Tecnologia de Alimentos , 10.1016 / j.tifs. 2020.10.036 , (2020) .
- Qiufen Li, Gen Wan, Chengying Peng, Lanjiao Xu, Yingmei Yu, Lin Li, Guanhong Li, Efeito da suplementação de probióticos no desempenho de crescimento, morfologia intestinal, integridade da barreira e resposta inflamatória em frangos de corte submetidos a estresse por calor cíclico , Animal Science Journal , 10.1111 / asj.13433 , 91 , 1 , (2020) .
- Simon Ghaly, Nadeem O. Kaakoush, Prue H. Hart, Efeitos da exposição UVR na microbiota intestinal de ratos e humanos , Photochemical & Photobiological Sciences , 10.1039 / C9PP00443B , (2020) .
- Peter I. Duncan, Olli Aitio, Annamari Heiskanen, Ritva Niemelä, Juhani Saarinen, Jari Helin, Nadine Porta, Muriel Fiaux, Denis Moënnoz, Mireille Golliard, Christine Cherbut, Rafael Berrocal, Sean Austin, Norbert Sprenger, Estrutura e Função de Bovine Whey Oligossacarídeos derivados que mostram propriedades protetoras da barreira epitelial simbiótica , nutrientes , 10.3390 / nu12072007 , 12 , 7 , (2007) , (2020) .
- Ningbo Wu, Dongping Chen, Hongxiang Sun, Jianmei Tan, Yao Zhang, Tianyu Zhang, Yuheng Han, Hongzhi Liu, Xinxing Ouyang, Xiao-Dong Yang, Xiaoyin Niu, Jie Zhong, Zhengting Wang, Bing Su, MAP3K2 aumenta a diferenciação celular Th1 via IL-18 para promover a colite mediada por células T , Science China Life Sciences , 10.1007 / s11427-020-1720-9 , (2020) .
- Madeline R. Barron, Roberto J. Cieza, David R. Hill, Sha Huang, Veda K. Yadagiri, Jason R. Spence, Vincent B. Young, The Lumen of Human Intestinal Organoids Poses Maior Stress to Bacteria Compar to the Germ-Free Ratinho Intestino: Escherichia coli Deficient in RpoS as a Colonization Probe , mSphere , 10.1128 / mSphere.00777-20 , 5 , 6 , (2020) .
- Lluïsa Miró, Concepció Amat, Cristina Rosell-Cardona, Joy M. Campbell, Javier Polo, Anna Pérez-Bosque, Miquel Moretó, Suplementação dietética com plasma porcino seco por spray atenua a inflamação do cólon em um modelo genético de doença inflamatória intestinal em camundongo , International Journal of Molecular Sciences , 10.3390 / ijms21186760 , 21 , 18 , (6760) , (2020) .
- Igor Splichal, Ivan Rychlik, Iva Splichalova, Daniela Karasova, Alla Splichalova, Receptor Toll-Like 4 Sinalização no íleo e cólon de gnotobióticos Leitões infectados com Salmonella Typhimurium ou seu isogênico Δrfa Mutantes , Toxinas , 10,3390 / toxins12090545 , 12 , 9 , (545) , (2020) .
- Fonte:https://onlinelibrary.wiley.com/doi/10.1111/imm.13117
Comentários
Postar um comentário